La afinidad eléctrica, afinidad electrónica, electroafinidad, AE o electron affinity es la energía intercambiada cuando un átomo neutro, gaseoso, y en su estado fundamental, capta un electrón y se convierte en un ión mononegativo. Es la cantidad de energía absorbida por un átomo aislado en fase gaseosa para formar un ión con una carga eléctrica de −1. Si la energía no es absorbida, sino liberada en el proceso, la afinidad electrónica tendrá, en consecuencia, valor negativo tal y como sucede para la mayoría de los elementos químicos; en la medida en que la tendencia a adquirir electrones adicionales sea mayor, tanto más negativa será la afinidad electrónica. De este modo, el flúor es el elemento que con mayor facilidad adquiere un electrón adicional, mientras que el mercurio es el que menos.

Dado que se trata de energía liberada, pues normalmente al insertar un electrón en un átomo predomina la fuerza de atracción del núcleo, tiene signo negativo. En los casos en los que la energía sea absorbida, cuando ganan las fuerzas de repulsión, tendrán signo positivo; la afinidad eléctrica se expresa comúnmente en el Sistema Internacional de Unidades, en kJ/mol.

Aunque la afinidad eléctrica parece variar de forma caótica y desordenada a lo largo de la tabla periódica, se pueden apreciar patrones. Los no metales tienen afinidades electrónicas más bajas que los metales, exceptuando los gases nobles que presentan valores positivos por su estabilidad química, ya que la afinidad electrónica está influenciada por la regla del octeto.
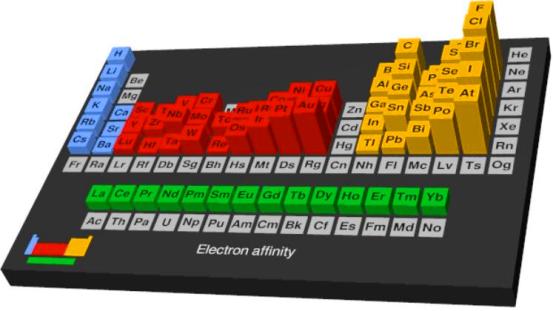
Los elementos del grupo 1, tienden a ganar un electrón y formar aniones −1, completando el subnivel s, mientras que los elementos del grupo 2, que ya lo tienen completo, no presentan esa tendencia. Análogamente sucede en el bloque p, donde las afinidades electrónicas se van haciendo más negativas a medida que nos acercamos a los gases nobles.
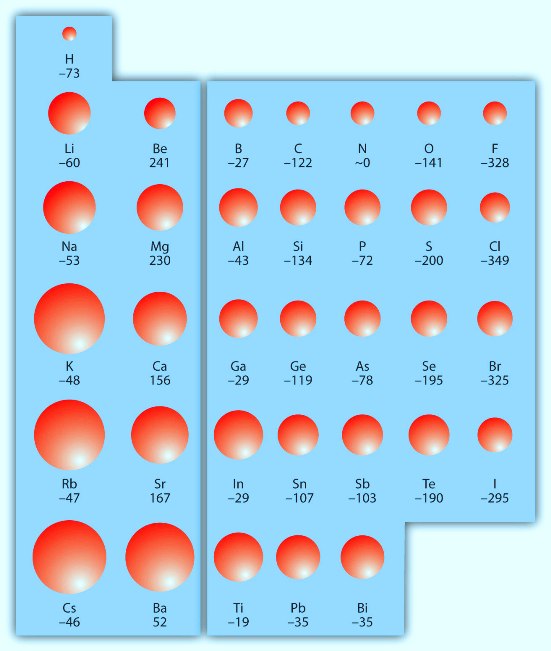
Afinidad Eléctrica en la tabla periódica. Los valores están expresados en KJ/mol.
Existen átomos que presentan capas de valencia con lugares vacantes o “huecos”, que pueden ser ocupados por electrones.
Entonces cuando a un átomo neutro se le añaden uno o más electrones se presenta un desprendimiento de energía, conocida como afinidad electrica, obteniéndose como resultado la formación de aniones.
Aunque la magnitud de dicha energía liberada sólo puede determinarse indirectamente y muy rara vez con gran exactitud, en la tabla periódica la podemos predecir en orden ascendente en un mismo período, de izquierda a derecha, y en un mismo grupo, de abajo hacia arriba.
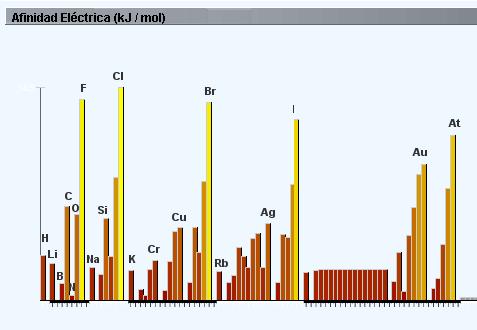
En síntesis: La afinidad eléctrica es la energía que se libera cuando un átomo de un elemento capta uno o varios electrones.
El átomo
En química y física, átomo (del latín atomus, y éste del griego άτομος, indivisible) es la unidad más pequeña de un elemento químico que mantiene su identidad o sus propiedades y que no es posible dividir mediante procesos químicos.
El concepto de átomo como bloque básico e indivisible que compone la materia del universo ya fue postulado por la escuela atomista en la Antigua Grecia. Sin embargo, su existencia no quedó demostrada hasta el siglo XIX. Con el desarrollo de la física nuclear en el siglo XX se comprobó que el átomo puede subdividirse en partículas más pequeñas.
La teoría aceptada hoy es que el átomo se compone de un núcleo de carga positiva formado por protones y neutrones, en conjunto conocidos como nucleón, alrededor del cual se encuentra una nube de electrones de carga negativa.
La tabla periódica de los elementos
La tabla periódica de los elementos es la ordenación que, atendiendo a diversos criterios, distribuye los distintos elementos químicos conforme a ciertas características.
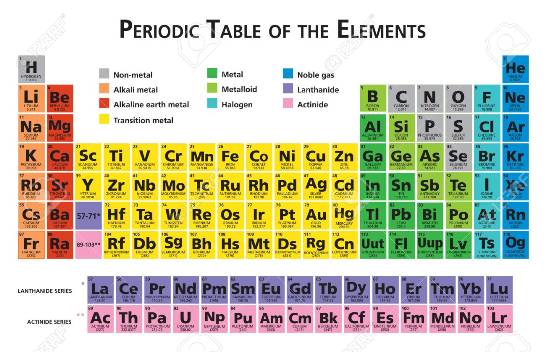
Suele atribuirse la tabla a Dimitri Mendeleiev, quien ordenó los elementos basándose en la variación computacional de las propiedades químicas, si bien Julius Lothar Meyer, trabajando por separado, llevó a cabo una ordenación a partir de las propiedades físicas de los átomos.
Los orígenes
Aunque algunos elementos como el oro, plata, estaño, cobre, plomo y Mercurio ya eran conocidos desde la antigüedad, el primer descubrimiento científico de un elemento ocurrió en 1669 cuando el alquimista Henning Brand descubrió el Fósforo.
El descubrimiento de la mayor parte de los elementos se llevó a cabo durante el siglo XIX; en 1830 ya se conocían 55 elementos. Un requisito previo necesario a la construcción de la tabla periódica era el descubrimiento de un número suficiente de elementos individuales, que hiciera posible encontrar alguna pauta en comportamiento químico y sus propiedades. Durante los siguientes 2 siglos, se fue adquiriendo un gran conocimiento sobre estas propiedades, así como descubriendo muchos nuevos elementos.

El concepto actual de elemento químico según la idea expresada por Robert Boyle en su famosa obra “The Sceptical Chymist”, “ciertos cuerpos primitivos y simples que no están formados por otros cuerpos, ni unos de otros, y que son los ingredientes de que se componen inmediatamente y en que se resuelven en último término todos los cuerpos perfectamente mixtos”, desarrollado posteriormente por Lavoisier en su obra “Tratado elemental de Química”, condujo a diferenciar en primer lugar qué sustancias de las conocidas hasta ese momento eran elementos químicos, cuáles eran sus propiedades y cómo aislarlos.
El descubrimiento de un gran número de nuevos elementos, así como el estudio de sus propiedades, pusieron de manifiesto algunas semejanzas entre ellos, lo que aumentó el interés de los químicos por buscar algún tipo de clasificación.
¿Y qué significa afinidad?
Afinidad significa proximidad, analogía, semejanza, parecido o parentesco de una cosa con otra. Por ejemplo, la afinidad entre dos lenguas como el portugués y el español. La palabra proviene del latín affinĭtas, affinitātis, que se refiere a ‘lo que es próximo’, ‘vecino’.
La afinidad es también un sentimiento de atracción, simpatía o compatibilidad de caracteres, opiniones, gustos entre dos o más personas. A nivel personal, la gente busca vincularse con quien tiene sentimientos de afinidad, así es como surgen el amor o la amistad. A nivel social, las personas tienden a agruparse según afinidades: políticas, deportivas, religiosas, filosóficas, profesionales.
Las otras afinidades
Afinidad Semántica
Como afinidad semántica nos referimos a las relaciones de proximidad o analogía que se establecen entre palabras de la misma categoría gramatical con significados que pueden ser parecidos, aunque no estrictamente idénticos. Las palabras en las que existe esta relación son conocidas como sinónimos, y son muy útiles a la hora de enriquecer el lenguaje o darle diferentes matices. Existen diferentes grados de afinidad semántica, por ejemplo, la que se identifica en palabras distintas que denotan estrictamente lo mismo: idioma = lengua; también puede ocurrir entre palabras que no siempre significan lo mismo, pero tienen un campo connotativo común: meta = objetivo; así como entre palabras que significan cosas opuestas pero, en determinados contextos, asumen otro valor semántico: “Felipe está dormido”, para referirse a que es muy listo, muy avispado.
Afinidad Electrónica
La afinidad electrónica, también conocida como electroafinidad, es la capacidad de los átomos para aceptar uno o más electrones. En este sentido, la liberación de energía que ocurre cuando un electrón es captado por un átomo en estado gaseoso determina su afinidad electrónica, que, de acuerdo con la Termodinámica, tiene un valor negativo. Mientras más negativa sea la afinidad electrónica, será mayor la tendencia del átomo para captar un electrón.
Afinidad en Farmacología
Dentro de la Farmacología, se llama afinidad a la capacidad de un fármaco para unirse con un receptor celular en el organismo y formar lo que se conoce como un complejo fármaco-receptor. En este sentido, es la afinidad determina el éxito de la acción farmacológica.
Afinidad en Química
Dentro de la Química, como afinidad se conoce la tendencia que dos o más elementos o compuestos químicos presentan para combinarse entre sí. Por lo tanto, cuando ocurre una combinación química, se atribuye la causa de este fenómeno a la afinidad que existe entre los componentes. Por ejemplo, la afinidad química entre los metales alcalinos y los elementos halógenos.

Afinidad en Derecho
En Derecho, como afinidad se designa el parentesco que un cónyuge contrae por matrimonio con los familiares por consanguinidad del otro. Vínculos de afinidad existen entre un yerno o nuera y sus respectivos suegros, así como entre cuñados. Este tipo de lazo es conocido como “parentesco político”. Así, el esposo de una tía pasaría a ser tío político del sobrino consanguíneo de la tía. El parentesco por afinidad no implica, por su parte, afinidad entre familiares consanguíneos de uno y otro cónyuge, por lo que se dice que “affinitas non parit affinitatem” (afinidad no crea afinidad).
Para el Derecho Canónico, la afinidad puede generar un impedimento para el matrimonio en el caso de que uno de los cónyuges pretenda contraer matrimonio con alguno de sus parientes por afinidad, en vista de lo cual, antes deberá regularizar su situación civil, sea esta de viudez o de divorcio.
Fuentes
Wikipedia: https://es.wikipedia.org/wiki/Afinidad_electr%C3%B3nica
“Afinidad”. En: Significados.com. Disponible en: https://www.significados.com/afinidad/
Fisicoquímica: http://www.quimicafisica.com/afinidad-electronica.html
Información relacionada
El bioetanol procedente de una hierba produce un 540% más de energía que la que consume
Más artículos sobre tecnología
Aƒƒinité électronique
